Harvardi Meditsiinikooli (HMS) ja MIT Üldhaigla ühine uurimisrühm ütleb, et nad on saavutanud mikrodiskilaseri väljundi häälestamise PEC-söövitusmeetodi abil, muutes uue nanofotoonika ja biomeditsiini allika "paljulubavaks".
(Mikrodiskilaseri väljundit saab reguleerida PEC-söövitusmeetodi abil)
Valdkondadesnanofotoonikaja biomeditsiin, mikrodiskettlaseridja nanodisk-laserid on muutunud paljulubavaksvalgusallikadja sondid. Mitmetes rakendustes, nagu kiibil olev footonkommunikatsioon, kiibil olev biokujutis, biokeemiline sensor ja kvantfootonite infotöötlus, peavad nad saavutama laseri väljundi lainepikkuse ja ülikitsasriba täpsuse määramisel. Siiski on sellise täpse lainepikkusega mikro- ja nanodisklaserite tootmine suures mahus keeruline. Praegused nanotootmisprotsessid toovad kaasa ketta läbimõõdu juhuslikkuse, mis raskendab lasermassi töötlemisel ja tootmisel kindla lainepikkuse saavutamist. Nüüd on Harvardi Meditsiinikooli ja Massachusettsi Üldhaigla Wellmani keskuse teadlaste meeskondOptoelektrooniline meditsiinon välja töötanud uuendusliku optokeemilise (PEC) söövitustehnika, mis aitab mikrodisklaseri laserlainepikkust täpselt subnanomeetrise täpsusega häälestada. Töö avaldati ajakirjas Advanced Photonics.
Fotokeemiline söövitamine
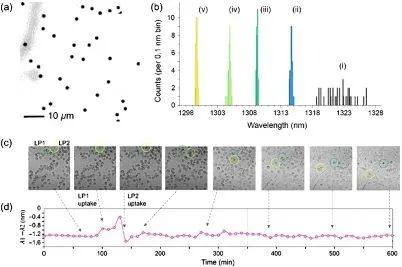
Aruannete kohaselt võimaldab meeskonna uus meetod toota mikroketaslasereid ja nanoketaslaserite massiive täpsete, etteantud emissioonlainepikkustega. Selle läbimurde võti peitub PEC-söövituse kasutamises, mis pakub tõhusat ja skaleeritavat viisi mikroketaslaseri lainepikkuse peenhäälestamiseks. Ülaltoodud tulemuste kohaselt sai meeskond edukalt indium-gallium-arseniidfosfaatmikrokettaid, mis olid kaetud ränidioksiidiga indiumfosfiidkolonni struktuuril. Seejärel häälestasid nad nende mikroketaste laserlainepikkuse täpselt kindlaksmääratud väärtusele, tehes fotokeemilise söövituse lahjendatud väävelhappe lahuses.
Samuti uurisid nad spetsiifiliste fotokeemiliste (PEC) söövituste mehhanisme ja dünaamikat. Lõpuks kandsid nad lainepikkusega häälestatud mikrodiski massiivi polüdimetüülsiloksaanalustmele, et toota sõltumatuid, isoleeritud laserosakesi erinevate laserlainepikkustega. Saadud mikrodiskil on ülilairibaline laserkiirguse ribalaius kooslaserkolonnil väiksem kui 0,6 nm ja eraldatud osakese suurus väiksem kui 1,5 nm.
Biomeditsiiniliste rakenduste ukse avamine
See tulemus avab ukse paljudele uutele nanofotoonika ja biomeditsiiniliste rakenduste jaoks. Näiteks võivad eraldiseisvad mikrodisklaserid toimida heterogeensete bioloogiliste proovide füüsikalis-optiliste vöötkoodidena, võimaldades märgistada spetsiifilisi rakutüüpe ja sihtida spetsiifilisi molekule multipleksanalüüsis. Rakutüübispetsiifilist märgistamist tehakse praegu tavapäraste biomarkerite, näiteks orgaaniliste fluorofooride, kvantpunktide ja fluorestseeruvate helmeste abil, millel on lai emissioonijoone laius. Seega saab korraga märgistada ainult mõnda spetsiifilist rakutüüpi. Seevastu mikrodisklaserite ülikitsa ribaga valguskiirgus suudab korraga tuvastada rohkem rakutüüpe.
Meeskond testis ja demonstreeris edukalt täpselt häälestatud mikrodiskilaseri osakesi biomarkeritena, kasutades neid kultiveeritud normaalsete rinnaepiteelirakkude MCF10A märgistamiseks. Oma ülilairibalise kiirgusega võivad need laserid potentsiaalselt revolutsiooniliselt muuta biosensorit, kasutades tõestatud biomeditsiinilisi ja optilisi tehnikaid, nagu tsütodünaamiline pildistamine, voolutsütomeetria ja multioomiline analüüs. PEC-söövitusel põhinev tehnoloogia tähistab suurt edasiminekut mikrodiskilaserites. Meetodi skaleeritavus ja selle subnanomeetriline täpsus avavad uusi võimalusi laserite lugematuteks rakendusteks nanofotoonikas ja biomeditsiinilistes seadmetes, samuti vöötkoodide loomiseks konkreetsete rakupopulatsioonide ja analüütiliste molekulide jaoks.
Postituse aeg: 29. jaanuar 2024





